資料來源與版權所有:肝病防治學術基金會
免疫療法與標靶治療 突破膽管癌治療困境!
諮詢╱林宗哲(臺大醫學院內科臨床副教授、臺大醫院癌醫中心分院腫瘤內科部主治醫師暨癌症防治中心主任 )
撰稿╱黃筱珮
有「隱藏版癌王」之稱的膽管癌,除開刀外,過去只有化療的選項,治療相當辛苦,療效也有限;近年膽管癌的免疫與標靶治療不斷有斬獲,為一些癌友爭取一線生機。
陳小姐因為腹部有點不適就醫,沒想到意外發現一顆很大的肝內膽管癌,讓她非常震驚沮喪。醫療團隊評估後為陳小姐進行手術治療以及輔助性化療,但仍於1年多後於肝內多處復發,並轉移至肺部, 接受化療後也沒有明顯起色。
原本已經束手無策的陳小姐,經醫師告知有一款針對膽管癌的標靶藥物即將健保給付,不過是針對膽管癌中有FGFR2基因變異者,而驗到這個基因變異的機會並不高,佔比只有10~15%。陳小姐不願放棄,決定自費10萬元接受NGS(次世代基因定序)檢測,幸運驗出腫瘤有FGFR2基因變異,可用pemigatinib標靶藥物精準治療,用藥後效果良好,腫瘤明顯縮小!愈來愈好的治療進展給陳小姐信心與希望,積極面對這場抗癌硬仗。
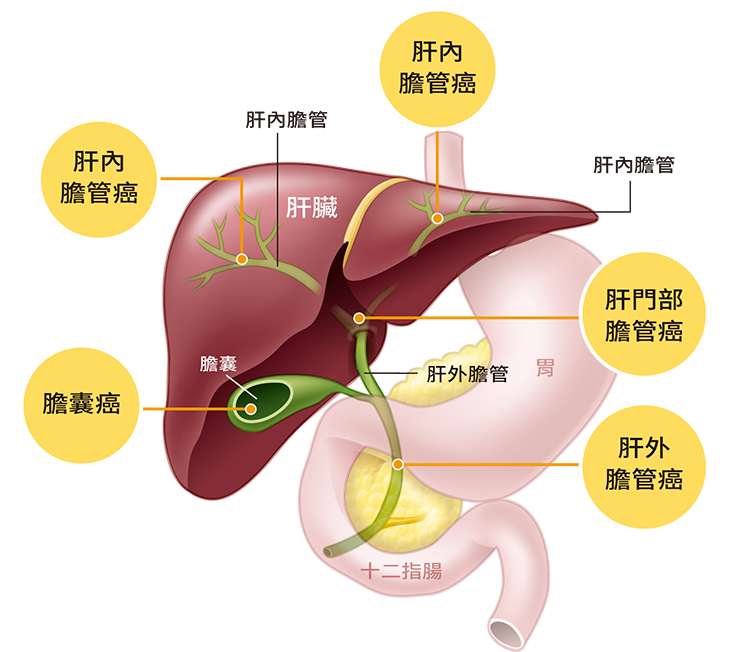
膽管癌又稱為「膽道癌」,可以發生在任何有膽管(道)的地方。膽管系統分布在肝臟內外,從肝細胞表面凹槽形成的微膽管開始,逐漸匯流成小膽管、左右肝內膽管,再穿出肝外合成為總肝管,與膽囊交匯後成為總膽管,最後流入十二指腸。
早期無明顯症狀 一發現多為晚期
依腫瘤發生部位,膽管癌又可細分為肝內周邊膽管癌、肝門部膽管癌、肝外膽管癌以及膽囊癌。
一般來說膽管癌早期並無特別症狀,一旦有黃疸、皮膚癢、體重減輕、食慾不振、發燒和腹痛等症狀時,多半已經晚期,常合併發生膽管阻塞情形。
膽管癌發生人數逐年攀升
危險因子較肝癌多且不明確
2020年台灣肝內膽管癌的粗發生率約為10萬分之5.98,而膽囊、肝外膽管及壺腹癌的粗發生率約10萬分之5.07;而比較10年間的發生人數,2010年時有975人罹患肝內膽管癌,2020年則有1411人,明顯逐年攀升。
為什麼膽管癌的發生有持續增加趨勢?推測與社會邁入高齡化、三高人口增加有關。
不過膽管癌的病因目前醫界還沒有定論。比較值得注意的是,因為飲食西化,三高(高血壓、高血糖和高血脂)的代謝症候群人口不斷增加,代謝症候群是許多癌症的危險因子,膽管癌也不例外,是否與膽管癌的發生率提高有關,值得觀察留意。
手術治療優先,但約7成無法開刀
一旦發現膽管癌,手術是最優先的治療方式,但因為膽管癌的早期症狀並不明顯,臨床上7成以上的患者一發現就是無法開刀的晚期,使得膽管癌被視為相當惡性的癌症,又有「隱藏版癌王」的稱號。
幸好近年無法手術的患者除了傳統化療之外,免疫療法和標靶治療也有相當令人雀躍的進展,對付膽管癌有更多新武器,不再只能望癌興嘆。
少數在可以開刀邊緣的腫瘤,可嘗試化療加放療作為開刀前的導引性治療;對於無法開刀的患者,化療是主要的治療方式,也可能視情況合併放療。常用的三類化療藥物是健擇(gemcitabine)、鉑類化合物(俗稱白金類,例如carboplatin、cisplatin等藥物)以及5FU類(包含靜脈注射劑與口服TS-1、capecitabine等)。
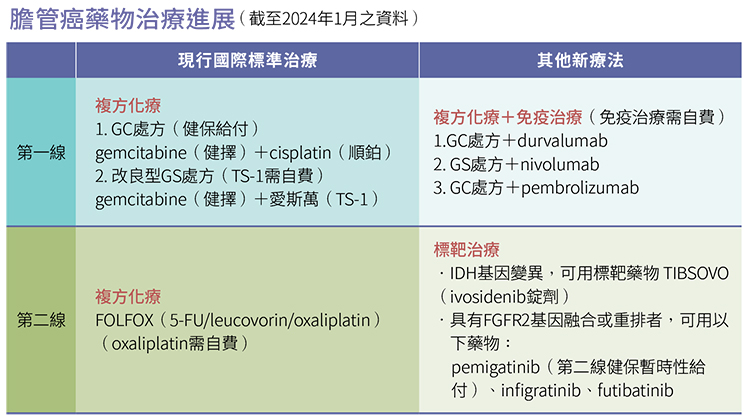
複方化療是第一線標準治療
目前膽管癌的第一線國際標準治療是從上述三類藥物中,選擇gemcitabine(健擇)搭配cisplatin(順鉑)的複方化療(簡稱GC),十多年前一項國際臨床試驗ABC-02顯示化療複方組合比單方好,約25%的膽管癌患者腫瘤明顯縮小,整體中位存活期11.7個月,該組合被大部分國際診療指引採用。
當第一線治療失效,第二線的化療標準改為FOLFOX(5-FU/leucovorin/oxaliplatin)的藥物組合,亦即以新一代白金藥物(例如oxaliplatin) 加5FU的複方療法。英國進行的ABC-06臨床試驗證實,FOLFOX相較於支持療法可以提高膽管癌治療的總存活期,6個月和12個月的總存活率都有臨床意義的改善。
由於白金類化療藥物副作用較強,使用「GC處方」約25%的病人會發生嚴重白血球低下的副作用,日本研究甚至高達60%會發生嚴重白血球低下。我國國衛院於2022年發表改良型「GS處方」,以每兩周注射一次的gemcitabine搭配每日口服愛斯萬(TS-1),臨床試驗發現與GC療法的療效相近,但只有4%的病人發生嚴重白血球低下的副作用,可考慮做為膽管癌第一線治療的另一個選擇。
免疫療法於膽管癌也具有明確角色
免疫療法用於膽管癌治療也有令人振奮的消息。過去免疫療法多半被用於後線的治療,但已有一些臨床試驗顯示,以化療為基礎,加上免疫療法合併用於第一線治療,可有效提升膽管癌病人的存活率,降低死亡風險。
2022年初的美國腸胃臨床腫瘤年會上,一個多國第三期膽管癌試驗(TOPAZ-1)也顯示,GC複方化療合併另一種免疫藥物durvalumab(PD-L1抑制劑),相較於傳統的GC療法,腫瘤反應率增加7~8%(中位數存活期變化),證明免疫搭配化療在膽管癌的治療效益。
2023年4月,美國癌症研究協會(American Association for Cancer Research, AACR)上,一個名為KEYNOTE-966跨國第三期臨床試驗的研究成果發表,再次證實免疫藥物在第一線膽管癌的治療效果。這項試驗是以GC化療合併使用免疫藥物pembrolizumab(PD-1抑制劑),結果受試患者的腫瘤反應率(腫瘤縮小)達29%、死亡風險降低2成左右;這相當程度與GC的複方化療合併免疫藥物durvalumab的試驗結果雷同。
先前國衛院研究團隊亦發表T1219第二期臨床試驗結果,使用改良型GS處方加上免疫治療藥物nivolumab(PD-1抑制劑)(簡稱NGS處方)。初步試驗結果顯示,在48名晚期膽管癌患者中,45%的病人腫瘤明顯縮小,整體中位存活期由傳統GC治療的11個月延長到19個月,且只有6%的病患發生嚴重白血球低下的副作用。
相較於化療併用免疫療法的效果,單用免疫藥物治療膽管癌的效果則不明顯,腫瘤反應率只有10%上下。由此看來,化療併用免疫療法做為晚期膽管癌第一線治療已有科學驗證,儘管健保尚未給付,不過愈來愈多病人願意自費接受治療,爭取更多生機。
肝內膽管癌基因突變多
標靶治療效果較好
除了免疫療法有所進展之外,膽管癌的標靶治療表現也愈來愈好。
過去膽管癌第二線治療以化療為主,通常存活期僅剩半年,現在還有愈來愈多標靶藥物可選擇。與傳統化療相比,這些標靶藥物通常能夠提供更好的治療效果,並提供更好的生活品質。
透過次世代基因定序(next generation sequencing, NGS)可以讓更多癌症突變基因現形,有將近50%的膽管癌可驗出變異基因。有鑑於膽管癌標靶治療的進步,醫界認為膽管癌的NGS納入健保給付確有其必要性,且應加快腳步。
不過,不同部位的膽管癌,基因突變情形也不一樣。肝內膽管癌的基因突變比例最多,高達一半以上,其中IDH(有分IDH1、2)突變佔15~20%,比例最高,國外已有對應的標靶藥物TIBSOVO(ivosidenib錠劑)上市,國內目前須專案申請自費使用;其次是FGFR2 基因的融合或重排等轉位,比例約10~15%,國內已有標靶藥物pemigatinib獲得健保第二線治療給付。另外HER2基因突變目前國外有雙特異性抗體藥物(抗體加標靶)在臨床試驗中,反應率有到4成。其他基因突變較少見,如RET基因、NTRK基因等。
肝外膽管癌的基因突變比例不高,IDH突變在肝外膽管癌約佔5%, 另有K-ras基因突變與p53基因失能表現,但後二者目前還沒有具顯著療效之標靶藥物可用。膽囊癌的基因突變相對多數是EGFR1、HER2基因突變,有些藥物可能可以嘗試。
FGFR2是目前膽管癌最常被討論的突變,已經有3種標靶藥物取得美國FDA核可,分別是pemigatinib、infigratinib以及futibatinib,能夠針對癌細胞中的特定分子或活化路徑進行抑制。其中pemigatinib臨床試驗顯示,腫瘤反應率可達到4成,存活期可拉長到17個月,對於有明顯腫瘤縮小的患者甚至可拉長到30個月。因此健保署於2023年5月已將此藥納入「暫時性給付」,若臨床療效良好,會考量常規給付,讓更多膽管癌病人受惠。
早期發現膽管癌
腹部超音波具有良好效益
膽管癌的治療較早年已有顯著的進展,不過在早期發現方面仍有許多挑戰待克服。所有癌症都一樣,早期發現、早期治療,預後最佳,但膽管癌早期症狀沒有特異性,抽血檢驗癌症指數,如癌性胚胎抗原(CEA)以及CA19-9,數值升高也不代表就是膽管癌。不過,腹部超音波對於膽管癌的早期發現具有相當好的效益,肝病防治學術基金會在近3年的全民腹超活動中,就發現2位無症狀的膽管癌病人,已順利接受治療。因此我們強烈呼籲40歲以上國人每年至少接受一次腹部超音波檢查,不只能守護肝臟健康,包括膽囊、脾臟、胰臟(雖然並非百分百)、腎臟、腹腔內的大血管以及淋巴結等器官組織的病變,也有機會及早發現異常,建議民眾可養成「一年一超」的習慣。
- Feb 18 Sun 2024 17:22
免疫療法與標靶治療 突破膽管癌治療困境!
close
全站熱搜
 留言列表
留言列表
發表留言


 留言列表
留言列表
 人電強身功
人電強身功 