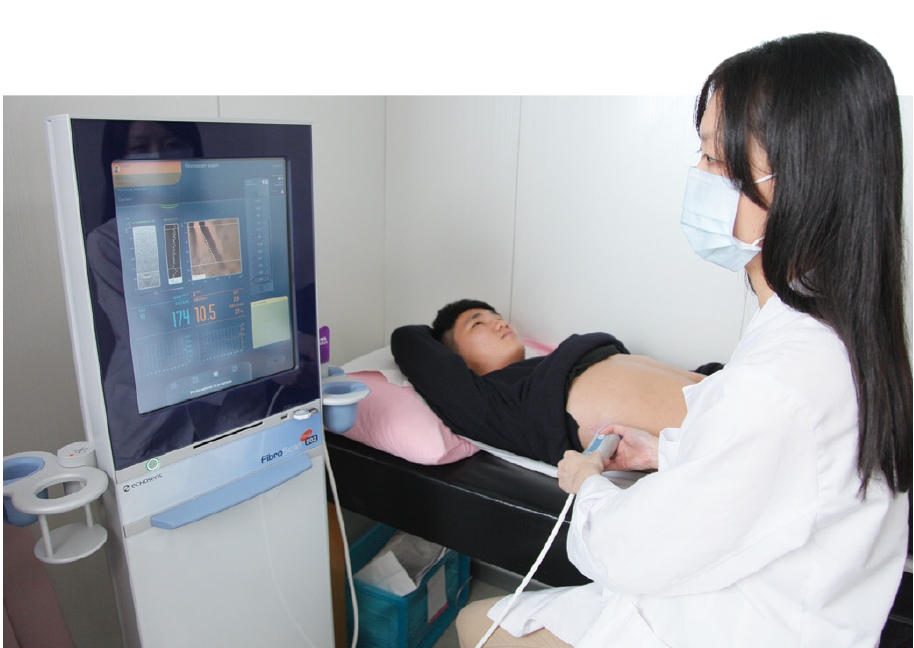
資料來源與版權所有:肝病防治學術基金會肝臟發炎可以吃B群嗎?撰稿/林姿伶(好心肝門診中心副院長、臺大醫院綜合診療部兼任主治醫師)每天的診間日常,最常見的主訴就是病人感到疲倦。會有這個問題的族群從青少年到90多歲的長輩都有,男性跟女性都會,比例大概佔了三分之一。而在肝病是國病的前提下,病人總覺得是肝臟出了毛病,所以接下來最常見的問題就是:「醫師,我是不是肝臟發炎?可以吃B群嗎?」「為什麼我吃了B群之後覺得噁心想吐、睡不著?」
疲倦原因很多 未必是肝臟出事其實,肝臟有沒有發炎,只要抽血,進行簡單的肝功能檢查就行了。可能令大家感到驚訝的是,雖然這麼多的病人覺得疲倦是自己肝臟出了問題,可是檢查出來的結果,肝發炎指數(AST、ALT)異常的比例只有一小部分。
疲勞感可能有多種不同的原因,比如說:急性及慢性疾病、過度工作、壓力和焦慮、睡眠不足、營養不足、缺乏運動等等,肝臟發炎只佔一小部分。
至於會有補充B群來改善疲倦的想法,是因為維生素B群在能量代謝、紅血球生成、神經系統功能等方面有重要的角色。而在都會區,因為飲食過度加工、飲食不均衡以及素食主義等因素,有些人可能會有維生素B6、B9(葉酸)、B12缺乏的問題。可是,參與能量代謝、能量生成,可能會對解除疲勞有幫助的卻是維生素B1、B2、B3、B5、B6,因此,對應上述都會區民眾飲食營養缺乏所致的疲倦感,似乎攝取B6就可以?而我們在藥局購買的B群補充劑,通常會包含維生素B1、B2、B3、B5、B6、B7、B9和B12,直接吃B群補充劑,就可以全包了?那麼,第一個問題來了,維生素B群明明是水溶性維生素,也就是說不易在體內累積,即使過量,理論上可以從尿液排除,為什麼有些民眾反應吃了之後反而會覺得噁心、想吐、睡不著呢?維生素B過量也有副作用事實上,即使水溶性維生素不易在體內累積,過量還是會有急性的毒性反應,就算可以從尿液排除,也需要一些時間。而補充維生素B群可能的副作用包括:腹痛和腹瀉、消化不良、過敏、感覺異常(B6)、神經疼痛(B6)、干擾其他維生素的代謝、影響癲癇藥物的效果等等;有時尿液會變黃(亮黃色)是因為高劑量維生素B2的關係。此外,因為補充維生素B會使得能量代謝提升、神經系統活躍,可能會增加身體的警覺性,部分人在晚上服用的時候,可能會干擾睡眠。
 肝臟發炎仍應先治本那麼,第二個問題是:「如果檢查出來的確是肝臟發炎,可以補充B群嗎?」肝臟發炎可以由多種因素引起,比如說脂肪肝炎、病毒感染(包括但不限於B肝跟C肝)、酒精濫用、藥物或毒素暴露等。維生素B群中的B1、B2、B3、B6、B9可能有助於恢復肝細胞功能、維持能量代謝,可是理應是屬於後線支援,如果導致肝臟發炎的病因不處理,反而治標不治本。而改善肝臟發炎的方法會建議從減少油跟糖等高熱量食物的攝取、避免含肝毒性成分的中草藥、西藥、偏方食品、減少酒精攝入、使用抗病毒藥物(對於病毒性肝炎)等著手。此外,在肝臟發炎期,也可能會影響營養吸收和代謝能力,對於營養補充劑的使用,必須非常謹慎。保肝藥的成分是什麼?
跟B群一樣嗎?當肝炎指數有偏高現象時,有些醫師也可能會開給病人肝臟庇護劑(俗稱保肝藥),例如以下兩種:水飛薊(Silymarin)這個藥物在臨床上常常被醫師拿來治療肝臟發炎,但算是「保護劑」,仍須先處理真正的病因,如酗酒、脂肪肝、病毒,否則無法「治本」。Silymarin是水飛薊(又名乳薊,為一種植物)的萃取物,算是一種中草藥材和食材,成分分析出來非常複雜,除了水飛薊素外還有幾種黃酮木酚。因為在實驗中發現可穩定肝細胞膜,因此被用作肝臟庇護劑。純粹的Silymarin是不包括維生素B的,可是因為很多藥品或營養補充品會加入維生素B群一起製作,因此在服用時也要注意可能有維生素B群補充相關的副作用。Procanpen這個也是在臨床上常常被醫師拿來治療肝炎的藥物,成分包括了膽鹼(維生素B4)、肌醇、半胱氨酸(一種胺基酸)、氰鈷胺素(維生素B12)。這個多成分的複合藥物嚴格來說算是一種含有膽鹼跟幾種維生素B的肝臟營養補充劑,跟坊間販售的維生素B群補充劑成分又有很大的不同。
肝臟發炎仍應先治本那麼,第二個問題是:「如果檢查出來的確是肝臟發炎,可以補充B群嗎?」肝臟發炎可以由多種因素引起,比如說脂肪肝炎、病毒感染(包括但不限於B肝跟C肝)、酒精濫用、藥物或毒素暴露等。維生素B群中的B1、B2、B3、B6、B9可能有助於恢復肝細胞功能、維持能量代謝,可是理應是屬於後線支援,如果導致肝臟發炎的病因不處理,反而治標不治本。而改善肝臟發炎的方法會建議從減少油跟糖等高熱量食物的攝取、避免含肝毒性成分的中草藥、西藥、偏方食品、減少酒精攝入、使用抗病毒藥物(對於病毒性肝炎)等著手。此外,在肝臟發炎期,也可能會影響營養吸收和代謝能力,對於營養補充劑的使用,必須非常謹慎。保肝藥的成分是什麼?
跟B群一樣嗎?當肝炎指數有偏高現象時,有些醫師也可能會開給病人肝臟庇護劑(俗稱保肝藥),例如以下兩種:水飛薊(Silymarin)這個藥物在臨床上常常被醫師拿來治療肝臟發炎,但算是「保護劑」,仍須先處理真正的病因,如酗酒、脂肪肝、病毒,否則無法「治本」。Silymarin是水飛薊(又名乳薊,為一種植物)的萃取物,算是一種中草藥材和食材,成分分析出來非常複雜,除了水飛薊素外還有幾種黃酮木酚。因為在實驗中發現可穩定肝細胞膜,因此被用作肝臟庇護劑。純粹的Silymarin是不包括維生素B的,可是因為很多藥品或營養補充品會加入維生素B群一起製作,因此在服用時也要注意可能有維生素B群補充相關的副作用。Procanpen這個也是在臨床上常常被醫師拿來治療肝炎的藥物,成分包括了膽鹼(維生素B4)、肌醇、半胱氨酸(一種胺基酸)、氰鈷胺素(維生素B12)。這個多成分的複合藥物嚴格來說算是一種含有膽鹼跟幾種維生素B的肝臟營養補充劑,跟坊間販售的維生素B群補充劑成分又有很大的不同。
跟營養補充劑維生素B群比起來,肝臟庇護劑經過實驗室證實對於肝炎是有療效的,因此若已診斷肝功能異常,比起自己買B群來吃,還是經醫師評估後使用肝臟庇護劑比較穩妥。最後,來回答這個主要的問題:肝臟發炎可以吃B群嗎?可以。不過要小心可能會出現維生素B群補充的相關副作用、毒性,以及一定要盡量找出肝臟發炎的原因來治療。維生素B群的補充可能是治標不治本,一旦有副作用或毒性的產生,必須立刻停止服用。而且,肝臟發炎不是自己可以感覺出來,唯有就醫檢查才能確定診斷。
vector 發表在
痞客邦
留言(0)
人氣()
資料來源與版權所有:健康醫療網
台灣C肝再治4.8萬人便達WHO目標 消除進度「C肝根除地圖」一目了然
記者吳儀文報導 2023-12-14
根據國健署資料顯示,C肝是僅次於B肝造成國人慢性肝炎、肝硬化與肝癌的主要原因。WHO所訂定之治療率目標為至少72%慢性C肝病人需被治療。國健署推估,台灣2025年的治療目標數約為23.7萬人,扣除目前估計已治療的目標族群約18.9萬人,預估再治療約4.8萬人,即可達到WHO的目標。
而國健署、台灣肝臟學術文教基金會、台灣消化系醫學會、台灣肝臟研究學會等也攜手合作,建立「臺灣C型肝炎根除地圖」網站,希望該網站能提升民眾對C肝的認知,成為台灣實現C肝根除目標的關鍵工具,並接軌國際分享台灣的策略、經驗和成果。

國健署、台灣肝臟學術文教基金會、台灣消化系醫學會、台灣肝臟研究學會等攜手合作,建立「臺灣C型肝炎根除地圖」網站。
推動C肝治療治療 擴大免費篩檢服務
為加強C肝防治,衛福部於2018年訂定「國家消除C肝政策綱領(2018-2025)」,將「以治療引領預防」、「以篩檢支持治療」、「以預防鞏固成效」作為政策方向,呼應世界衛生組織(WHO)提前消除病毒性肝炎的計畫性目標。
在治療的部分,健保署自2003年10月起開始推動C肝治療計畫,並實施C肝感染者醫療給付方案,約有8萬人透過干擾素治療成功,另外自2017年起健保開始提供的C肝病人免費C肝全口服新藥治療,截至今年8月止,共治療15.7萬人,平均治療成功率達98.4%。
針對篩檢的部分,國健署為篩出慢性C肝病人,自2011年8月開始提供民國55年次(含)且滿45歲的民眾終身1次B、C 肝免費篩檢服務,並在2020年9月起開始擴大篩檢年齡。
目前,45-79歲民眾、40-79歲原住民只要符合篩檢資格,進到成人預防保健特約醫療院所,都可以接受C肝篩檢。國健署表示,截至今(2023)年8月止,累計篩檢人數(包括非成健篩檢管道)已超過540萬人。
建立「C肝根除地圖」 分享國內根除策略與成果
另外,台灣肝臟學術文教基金會也與國健署、台灣消化系醫學會、台灣肝臟研究學會等合作建立一個線上數位生態系統「臺灣C型肝炎根除地圖」網站(網址:https://www.taiwan-hcv-elimination.org/)。
國健署表示,該網站由中山大學醫學院余明隆副校長主持,為台灣醫療專業人員、政策制定者和公眾建制了一個清晰的模式,提供台灣最新的C肝根除數據,同時提升民眾對C肝的知識。
除此之外,網站也致力於接軌國際,分享台灣的策略、經驗和成果。國健署提到,這不僅是台灣實現C肝根除目標的關鍵工具,也為其他國家提供成功的C肝防治範本,期待在各界共同努力下,積極擴大C肝篩檢涵蓋率,及早找出C肝病人進行治療。
吳昭軍署長也呼籲,民眾若符合C肝篩檢資格,應主動接受篩檢,篩檢C肝抗體陽性者,應進一步接受C肝病毒檢測,如果C肝病毒檢測陽性,應積極接受治療,以降低未來發生慢性肝炎、肝硬化及肝癌風險。-----------------------------------資料來源與版權所有:健康醫療網
3步驟預防C肝!「這族群」可免費篩檢 20萬治療藥物全額健保給付
記者吳儀文報導 2023-12-04
根據國健署資料顯示,C肝是僅次於B肝造成國人慢性肝炎、肝硬化與肝癌的主要原因。WHO所訂定之治療率目標為至少72%慢性C肝病人需被治療。國健署推估,台灣2025年的治療目標數約為23.7萬人,扣除目前估計已治療的目標族群約18.9萬人,預估再治療約4.8萬人,即可達到WHO的目標。
而國健署、台灣肝臟學術文教基金會、台灣消化系醫學會、台灣肝臟研究學會等也攜手合作,建立「臺灣C型肝炎根除地圖」網站,希望該網站能提升民眾對C肝的認知,成為台灣實現C肝根除目標的關鍵工具,並接軌國際分享台灣的策略、經驗和成果。
國健署提供45-79歲民眾終身一次B、C型肝炎篩檢,目前全國約5,400家醫療院可提供B、C型肝炎篩檢服務。
根據國健署資料顯示,國內每年因慢性肝病、肝硬化及肝癌死亡人數超過萬人。許多人都知道預防B型肝炎很重要,但除了B肝外,事實上C肝預防也不可輕忽。國健署鼓勵,民眾可善用B、C型肝炎篩檢服務,並做好C型肝炎防治3步驟,一同為消除C型肝炎的目標努力。
肝病早期無症狀 應善用B、C肝篩檢早發現早治療
肝病早期通常沒有明顯症狀,一旦有症狀時,大多已是肝病晚期。目前國健署提供45-79歲民眾終身一次B、C型肝炎篩檢,截至112年7月曾接受過篩檢的人數已經超過533萬人。國健署署長吳昭軍表示,鼓勵符合條件的民眾,為了自己也為了家人,善用政府提供的免費服務。
從111年3月1日起放寬成人預防保健服務特約醫療院所的專科醫師都可提供服務,不限於內科或家醫科,估計有3.5萬名醫師投入,目前全國約5,400家醫療院可提供B、C型肝炎篩檢服務。而國健署也持續研議推出醫療院所補助措施,以提升醫療院所及專科醫師的參與意願,增加民眾接受篩檢的可近性。
國健署表示,本項政策推動不只是照護國民健康,也呼應世界衛生組織(WHO)2030年消除病毒性肝炎目標,期望透過民眾、醫療團隊與政府的共同努力,台灣能提早於2025年消除C型肝炎,取得WHO消除C肝認證,突顯我國於公共衛生管理上之國際地位。
3步驟防治C肝 藥物全額健保給付治癒率逾9成
不過,國健署發現,自100年起提供篩檢服務,45-79歲接受B、C型肝炎篩檢人數已累計達533萬人,其中C肝抗體陽性率為2.8%,陽性個案之病毒量檢驗率為72%,進一步檢測出C型肝炎病毒量(HCV RNA)陽性為44.3%,參與直接作用抗病毒藥物治療率為91.5%。
國健署表示,由於C型肝炎的治癒率高達98%,而且其中治療所需的藥物費用20萬元由健保給付,因此提醒民眾及早篩檢以了解自己的健康狀況,若發現為C型肝炎患者,應配合治療,此外也提醒民眾以下3步驟防治C型肝炎:
第一步:避免接觸危險因子,如:穿耳洞、刺青工具等需充分消毒滅菌,避免不必要的輸血、打針、針灸、刺青、穿耳洞等行為;養成良好個人衛生習慣,不與別人共用針具、刮鬍刀、牙刷、指甲剪;不從事無保護的性行為。
第二步:及早篩檢,一生至少接受1次B、C型肝炎篩檢。
第三部:配合治療,如篩檢陽性者及早就醫,定期追蹤及治療。
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
資料來源與版權所有:肝病防治學術基金會胰臟癌治療新觀念
複方化療後再手術 提升存活率諮詢╱吳健暉(臺大醫院一般外科及胰臟癌精準醫療中心主治醫師)
撰稿╱黃筱珮面對有「癌王」之稱的胰臟癌,能夠直接開刀算是幸運的患者,因為只有開刀能有機會治癒胰臟癌;不過第三期也不用太灰心,接受先導性化療讓腫瘤縮小,也能迎來手術機會。 60多歲劉先生因上腹痛、加上兩個月內掉了10公斤,在太太陪同下前往醫院檢查,確診為第三期胰臟癌。被檢出「癌王」的劉先生一時之間難以接受,覺得人生無望,但在太太鼓勵與醫師建議下,決定接受化療組合藥物的前導性治療,4個月後腫瘤縮小,順利接受手術,至今2年多時間過去,他恢復良好,經常與家人出國旅遊,得來不易的每一天都充滿感激。胰臟位在腹腔深部,體積小,很容易被忽略,卻是人體唯一同時具有內分泌和外分泌功能的重要器官。早期的胰臟癌沒什麼症狀,當腫瘤漸漸擴大,就會陸續出現上腹痛、體重減輕、黃疸等症狀,也可能有背痛、腹脹、噁心嘔吐、血糖升高、脂肪便、長期慢性腹瀉等症狀。
60多歲劉先生因上腹痛、加上兩個月內掉了10公斤,在太太陪同下前往醫院檢查,確診為第三期胰臟癌。被檢出「癌王」的劉先生一時之間難以接受,覺得人生無望,但在太太鼓勵與醫師建議下,決定接受化療組合藥物的前導性治療,4個月後腫瘤縮小,順利接受手術,至今2年多時間過去,他恢復良好,經常與家人出國旅遊,得來不易的每一天都充滿感激。胰臟位在腹腔深部,體積小,很容易被忽略,卻是人體唯一同時具有內分泌和外分泌功能的重要器官。早期的胰臟癌沒什麼症狀,當腫瘤漸漸擴大,就會陸續出現上腹痛、體重減輕、黃疸等症狀,也可能有背痛、腹脹、噁心嘔吐、血糖升高、脂肪便、長期慢性腹瀉等症狀。
因為胰臟癌發現時多已晚期,是消化系癌症中療效和預後最差的疾病之一,死亡率一直居高不下。根據衛福部統計,國內111 年胰臟癌死亡人數 2,769 人,較前一上年上升 4.1%,死亡率為每十萬人口 11.9 人,亦較前一上年上升 5%,順位由第 9 位上升至第 7 位;若與十年前(民國101年)年比較,胰臟癌死亡人數及死亡率分別上升 67.1% 及 67.6%。
發現胰臟癌 僅兩成可開刀
近年胰臟癌發生人數也有攀升趨勢,國內目前每年新增約3~4千名患者。統計顯示,確診胰臟癌時,只有約20%是可以開刀的早期患者,80%病人腫瘤已經有局部侵犯甚至遠端轉移,所以無法立刻開刀,其中已轉移的第四期約佔50~60%,20~30%屬於沒轉移但有局部血管侵犯的第三期,稱為「局部侵犯嚴重型」,這期病人雖然無法立刻開刀,但仍然可以積極治療,爭取生機。前導性治療 有效提高存活率
胰臟癌一旦有明顯的上腹疼痛、黃疸等狀況,通常癌細胞已侵犯到鄰近血管(第三期)或轉移到其他器官(第四期),這時就無法動手術。
不過,第三期和第四期的治療方式和存活率並不相同,第四期病人通常只能接受化療,如果反應不好,平均存活期大約3到6個月;而針對局部侵犯嚴重型的第三期患者,美國自十幾年前開始建議做「前導性治療」,有效的話,腫瘤縮小,就能順利銜接手術(此一策略又稱轉化性手術),就有機會延長生命,甚至達到治癒可能。臨床經驗顯示,胰臟癌只有開刀才有治癒可能,如果只做放療或化療,基本上不可能治癒。
所謂的第三期胰臟癌前導性治療,美國常用的第一線處方有兩種。在臺大醫院的流程中,第一階段先讓病人接受名為FOLFIRINOX的複方化學治療,主要包括5-FU、irinotecan與oxaliplatin等3種化學治療藥物,在合併使用下可大幅增加胰臟癌腫瘤縮小的機會。
對於FOLFIRINOX有效的病患會繼續使用原本處方進行4~6個月的治療。在美國與臺大的治療經驗中,有一種稱為處方轉換的策略。對於第一階段治療反應不佳的病患,兩個月後換藥,第二階段換用亞伯杉(Abraxane)併用健擇(gemcitabine)的化療藥物組合,接續治療兩個月,這樣有機會增加反應率。完成總計4個月的前導性治療後,腫瘤有效穩定控制約為6~7成、病人能開刀比例超過2成,大幅提高存活率。臺大經驗:標準化流程的前導性治療後26%可手術臺大醫院參照美國醫界的做法,收治胰臟癌患者後,會先進行電腦斷層(CT)、磁振造影(MRI)、正子掃描(PET)及腫瘤標記等檢查,確認為第三期局部嚴重侵犯型的患者,會建議患者以FOLFIRINOX複方的化療處方開始前導性治療,兩個月後進行評估,若是FOLFIRINOX有效,則繼續治療兩個月;若是FOLFIRINOX無效,會評估進行處方轉換,建議患者採用亞伯杉(Abraxane)併用健擇(gemcitabine)的藥物組合,再治療2~4個月後評估能否手術。必要時會追加前導性放射線治療。
由於目前健保僅給付上述化療組合藥物於第四期轉移性的胰臟癌患者,因此第三期患者若要接受前導性治療必須自費。FOLFIRINOX一個月藥費約3~5萬元、健擇加亞伯杉注射劑一個月則要將近5~10萬元,病人是否接受前導性治療、以及是否要選擇轉換處方,經濟負擔也是重要考量。
依據臺大醫院經驗,從2017年至今,接受前導性治療的胰臟癌患者從29歲到90多歲都有,8成完治的患者之中,有26%可順利接受手術,有一部分是前導性治療後即能手術,術後再做化療與放療,以及低劑量的維持性化療;有一部分則是完成前導性治療後,還需要再做兩個月化療以及6周放療才能順利手術,這些能夠開刀的患者,存活時間都遠比原本預期的9個月長,有些能夠長達數年,甚至達到永久性存活(治癒)。術後輔助性化療可減少復發術後是否要接受輔助性化療視病人情況而定,有淋巴結轉移或神經叢侵犯,基本上都一定要做;若是無淋巴結轉移或無神經叢侵犯,臺大醫院的作法是減藥或縮短時間,以減少復發的機率。
另外有21%的患者在前導性治療後腫瘤穩定控制,雖然評估後仍然無法開刀,不過接續放射線治療以及維持性化療,存活率也有改善。
整體而言,台灣的胰臟癌病人接受前導性治療的比例及療效不及美國,主要是藥費昂貴與化療耐受度的差異,即便如此,對於胰臟癌晚期、無法開刀的患者來說,仍是提高存活率的一線生機。標準化的前導性治療療程、有經驗的決策和團隊合作都會提升治療成績。內視鏡超音波 不建議單獨做為健檢或篩檢胰臟癌工具
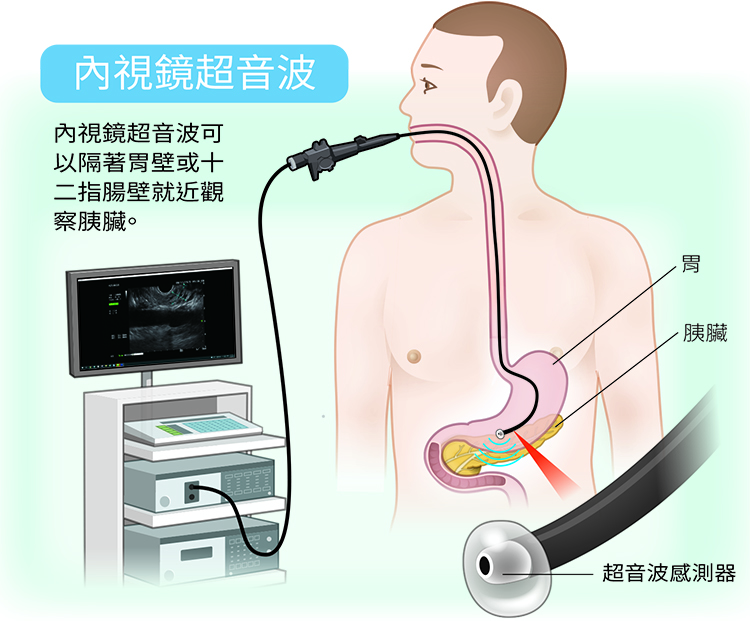 前導性治療帶給第三期胰臟癌治療新契機,不過若能早期發現當然更好,因此許多人都會期待是否有任何檢查可以及早發現胰臟病變。不具侵入性的腹部超音波在檢查胰臟時,因容易被腸氣擋住,看不清楚,所以不是一個很好的篩檢胰臟癌工具;有些醫療院所將內視鏡超音波(EUS)列為篩檢胰臟癌的項目,EUS雖然可以檢查胰臟,但這是類似胃鏡的檢查,是在內視鏡的前端增加一個超音波偵測器,從病人嘴巴深入食道、胃部,隔著胃壁或十二指腸壁就近觀察胰臟,具侵入性,有一定的風險。
前導性治療帶給第三期胰臟癌治療新契機,不過若能早期發現當然更好,因此許多人都會期待是否有任何檢查可以及早發現胰臟病變。不具侵入性的腹部超音波在檢查胰臟時,因容易被腸氣擋住,看不清楚,所以不是一個很好的篩檢胰臟癌工具;有些醫療院所將內視鏡超音波(EUS)列為篩檢胰臟癌的項目,EUS雖然可以檢查胰臟,但這是類似胃鏡的檢查,是在內視鏡的前端增加一個超音波偵測器,從病人嘴巴深入食道、胃部,隔著胃壁或十二指腸壁就近觀察胰臟,具侵入性,有一定的風險。
此外,有些民眾在接受EUS篩檢後,被告知檢出IPMN(分支胰管型乳突內瘤),IPMN可能是胰臟癌的癌前病變,民眾焦慮心情可想而知,因此趕緊到醫學中心掛門診,但是進一步檢查有不少其實是「偽陽性」(沒有此一病灶)。主要是EUS的檢查有一定的技術難度,判讀病灶也有檢查者主觀的成分在,而且EUS屬於侵入性的檢查,有可能造成胃腸穿孔的風險,因此是否要拿來作為針對一般人的健檢或篩檢工具,仍有爭議。原則上並不建議常規在健檢單獨使用篩檢胰臟癌,以免造成不必要的焦慮與醫療浪費。高風險族群較建議檢查
若想要檢查是否有胰臟癌,在高風險族群會建議以電腦斷層(CT)或磁振造影(MRI)檢查為主,若是具有胰臟癌家族史或BRCA基因缺陷的高風險族群,美國約翰霍普金斯大學醫學院建議做MRI和EUS;臺大醫院針對胰臟癌的高風險族群,首次檢查也是MRI和EUS一起做,之後就用MRI追蹤。美國梅約診所則建議新發生的糖尿病患者都應該留意是否有胰臟癌的可能性。
面對胰臟癌的威脅,要小心但不要過度擔心。坊間健檢常有腫瘤指標CA19-9、CA125、CEA、CA153等項目,但這些項目數值異常,可能的原因非常多,不代表就是胰臟有問題;如果數值異常一直找不到原因,醫師會進一步安排CT或MRI檢查,若仍查不到病灶,可以考慮自費接受PET檢查,以確認是否跟胰臟癌有關。
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
資料來源與版權所有:肝病防治學術基金會翻轉晚期肝癌 釔90微球體 「體內放療」
殲滅肝腫瘤諮詢/吳志宏(臺大醫院影像醫學部主治醫師、臺灣介入放射線學會秘書長)
撰稿/楊雅馨釔90微球體也是放射治療的一種,但放射物質是包覆在一個極小的球體內,透過血管送達腫瘤部位,在體內直接殲滅癌細胞!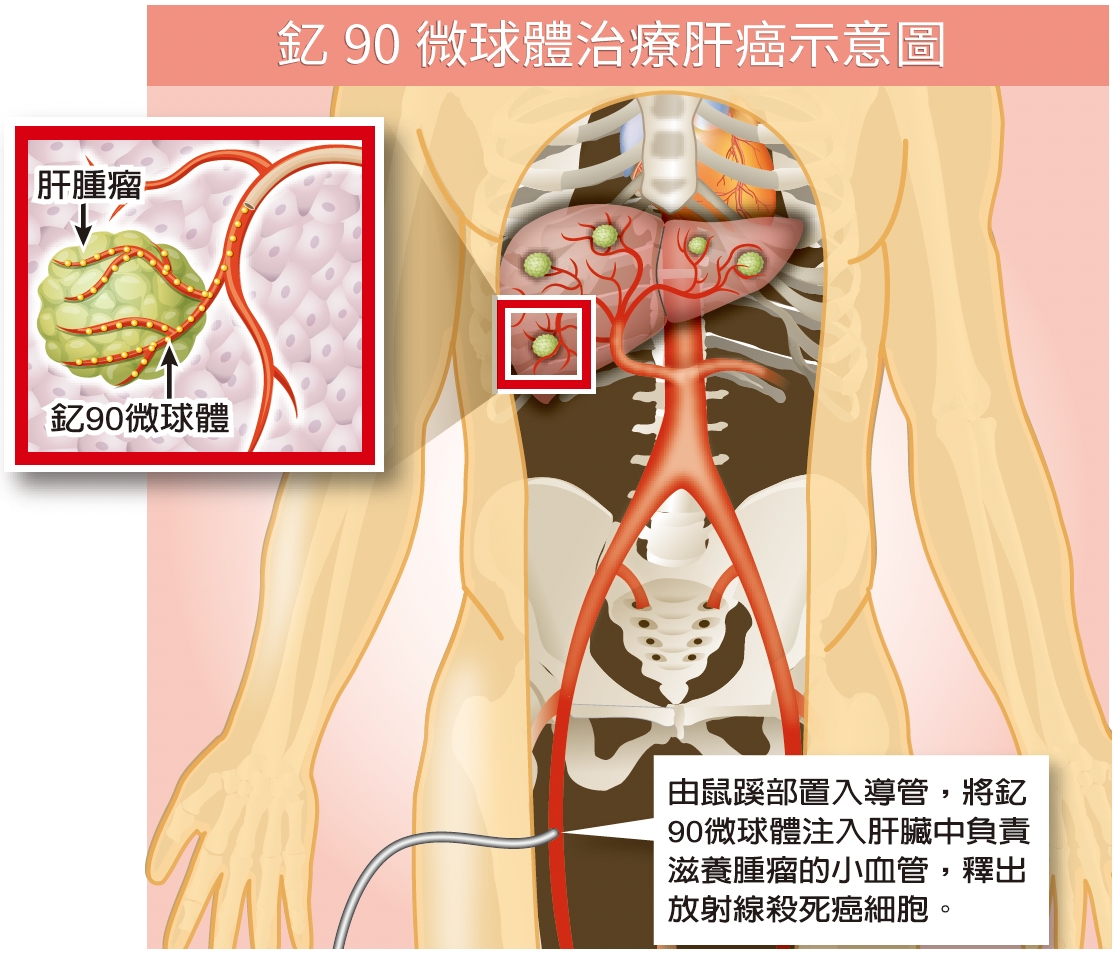
圖說:釔90微球體治療肝癌示意圖一名65歲女士罹患肝癌,接受手術治療,原以為從此可高枕無憂,沒想到多年後肝癌竟復發且腫瘤已大到11公分,由於剩下的肝臟有限,無法再手術,醫師建議接受「釔90微球體體內放射治療」, 6個月後腫瘤縮小至6公分,緊接著再進行「微波消融術」破壞腫瘤,如今,肝腫瘤成功獲得控制,已經超過3年。釔90是以一種「微球體」包覆放射物質,透過肝動脈栓塞方式將微球體運送到肝腫瘤處,在病人體內釋放出β射線,進而殺死肝腫瘤。放射線所影響的範圍只有腫瘤及其周邊一公分左右,所以對正常組織傷害很小。
微球體的材質有樹脂(resin yttrium 90)、玻璃(glass yttrium 90)等兩種,以往只有樹脂型,後來又多了玻璃型,後者能夠提供的輻射劑量比較高,更適合用於治療原發性肝癌。微球體的體積很小(樹脂20~60 μm,玻璃25 μm),只有約兩倍白血球的大小,在血管裡不會有卡住的問題,但也因體積小、容易隨著血流飄移出去,因此,在治療前要精準計算病人肝臟、肺臟的血流分流情形,評估可能流到肺部的劑量多寡。
與其他放射治療的差別
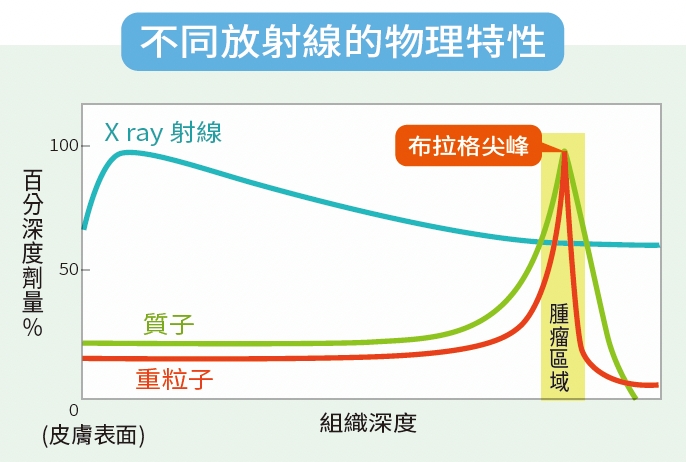
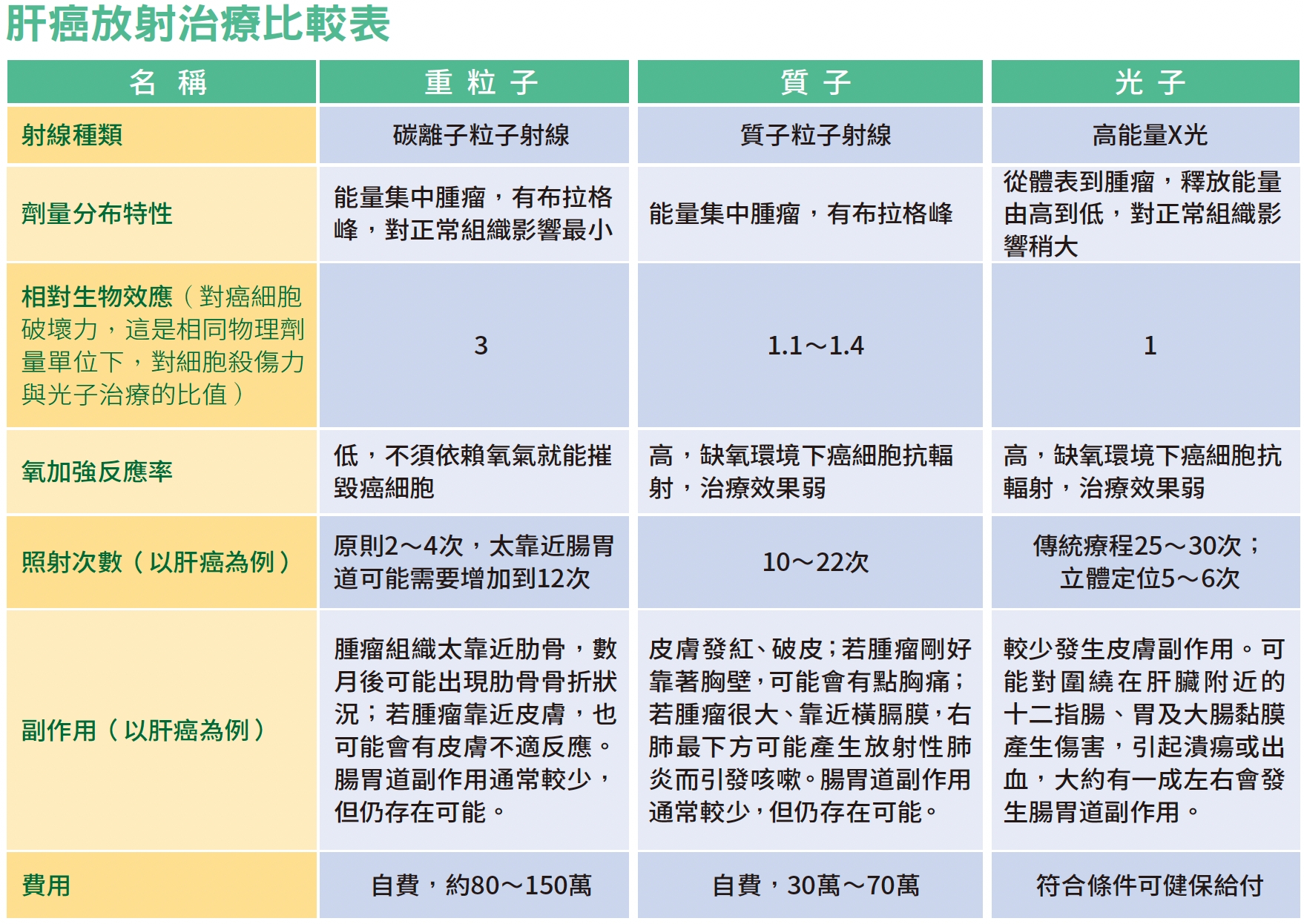
同樣是放射療法,釔90與其他放射線療法最大的不同就是從「體內」往體外治療,不會影響皮膚;而光子、質子、重粒子等放射線治療,則是由體表往體內照射,對皮膚及射線經過的器官多少會有影響。除光子治療有健保給付外,釔90、質子、重粒子皆屬自費療程。此外,光子、質子、重粒子都需要多次的照射,好處是不需要住院、不用打針;釔90最大的優點是只需要一次療程,但需住院治療。費用約60萬元~70萬元不等。
這幾種放射治療究竟哪一種療效最好?目前並沒有直接比較的臨床試驗,所以沒有這方面的數據,醫師通常根據病人病況、條件及意願提供意見。例如,若病人不希望多次治療的話,只需要治療一次的釔90,可能是比較方便的選擇。釔90治療後
兩成病人肝腫瘤縮小、降期接受釔90治療,有機會把肝癌分期降期(downstage)。臺大醫院曾統計2010到2019年這10年間利用釔90治療原發性肝癌共約100例的經驗。臨床統計顯示,約有20%的病人可以成功降期去接受肝臟手術、肝臟移植、無線射頻消融(俗稱電燒)等根除性療法,而病人的甲型胎兒蛋白(AFP)低於400 ng/mL以下,是一個可以降期的重要決定因素。
不過,接受釔90治療後的銜接治療,除了免疫治療不需要「等待期」外,其餘的相關治療如手術、移植、無線射頻消融等,都建議於半年後再進行,其目的是為了等待釔90療效產生。
依據臺大醫院的經驗,營養狀況好(無肌少症)的病人,釔90治療後的中位數整體存活期(median overall survival)為24個月,營養狀況較差(有肌少症)者為15個月。存活期也有男女的差異,女性為24個月,男性是15個月。治療完後腫瘤會縮小的機率為40%。
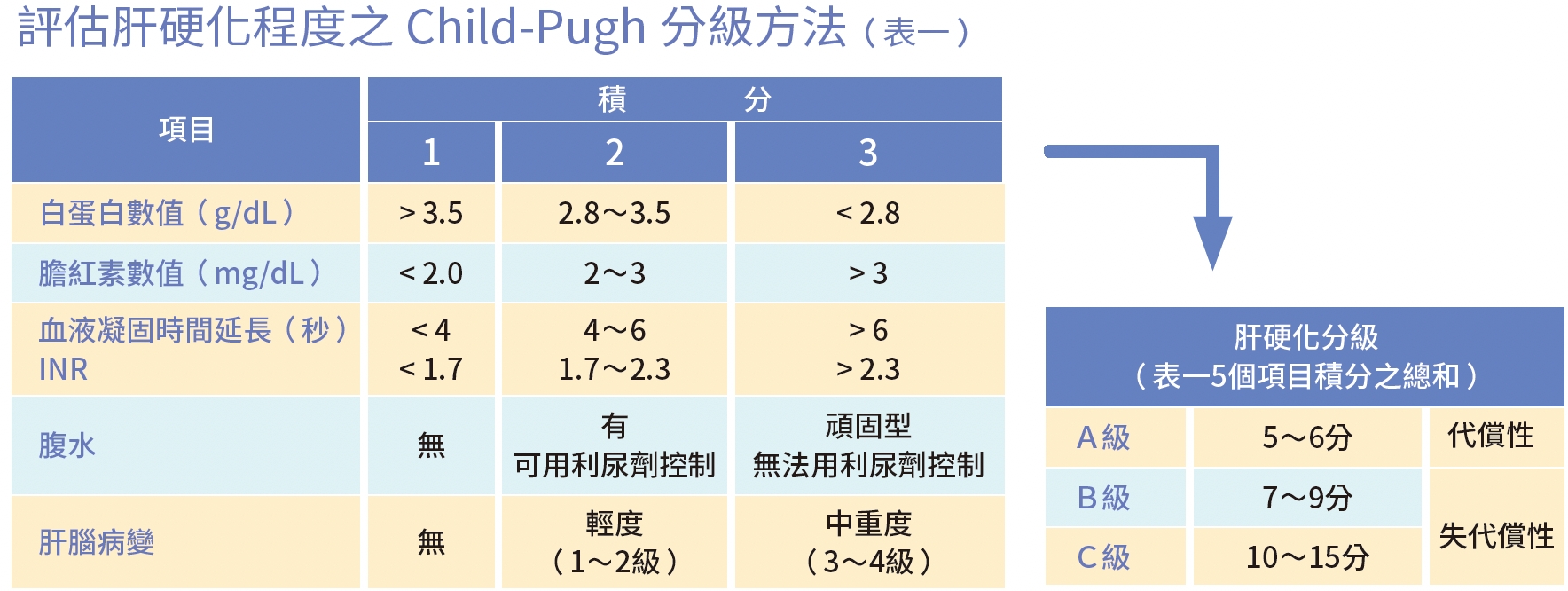
釔90治療之適應症及禁忌至於哪些病人適合使用釔90治療?一般來說,肝癌分期屬於B、C期,對於栓塞或標靶藥物治療效果不佳者;想接受肝臟移植卻不符合米蘭標準(Milan criteria)或美國加州大學舊金山分校(University of California San Francisco, UCSF)標準;肝功能狀況依據Child-Pugh Score分為A、B、C等級,肝功能A級及一部分B級(7分以上)的病人可以做,但若病人有腹水就不適合。
由於肝臟接受放射劑量是有上限的,劑量加總起來需在40 Gy(葛雷)以下,所以如果病人的肝臟曾接受任一種放射線治療,就不能再做釔90。肝臟曾接受其他治療(如手術、電燒、標靶、免疫療法等)則不受限制。
其他禁忌症還包括:黃疸高於1.5 mg/dL、有急性肝炎、腹水者;目前有在使用標靶藥物Avastin(癌思停)者,需先停藥6周。術前需先評估
治療過程需住院做釔90治療前需先評估,此項評估會在核子醫學部執行,模擬放射物質到達肝臟後,有多少會在肝臟吸收,多少比例會隨血流跑到肺部,流到肺部的比例應少於10%,換句話說,留在肝臟要有90%左右,才適合接受此項治療。因為一旦放射物質跑到肺部,會造成「間質性肺炎」,需使用類固醇治療,而且很難處理。
一般來說,肝腫瘤太大、有門靜脈主幹侵犯者,採釔90治療對肺部的影響可能比較大,就不適合。
當評估階段的模擬結果符合治療標準,即可進入治療階段。治療方式與肝動脈化學栓塞的做法一樣,醫師會將導管由病人鼠蹊部進入股動脈,做血管攝影,然後深入腹主動脈,直接進入到肝腫瘤所在的動脈分支,再把釔90微球體注入至肝臟腫瘤處,在極近的距離內將高劑量的輻射給予腫瘤,殺死癌細胞。手術時間約1.5~2小時,不需全身麻醉。釔90相對於傳統栓塞,副作用較低,治療侷限在肝臟部位,病人治療後大多沒有特別不適反應。
不過,釔90需一周時間才會衰變完畢,因此術後建議病人住單人房,一周內避免與小孩及孕婦接觸。合併免疫療法
盼提高肝癌治癒率晚期肝癌的第一線療法除標靶藥物外,還有免疫加標靶的選項,也是近年來很大的突破,免疫治療需要抗原才能激發免疫反應,而接受像釔90這類的放射治療後,腫瘤細胞(抗原)還在,只是壞死,所以有些理論認為抗原還在的情況下接受免疫治療,免疫效果可能會增強。
目前已知以釔90對付肝腫瘤,有20%的機率可以銜接開刀或電燒等達到治癒性治療,若合併免疫治療或許可以將機率提高到40%。所以目前也有「釔90微球體放射治療後合併免疫加標靶(atezolizumab+bevacizumab)」的臨床試驗在進行中,期待透過免疫療法的加成,提高肝癌治癒率。
疑 惑 解 除 補 給 站
Q:原本不能開刀,為什麼接受釔90微球體放射治療後,有機會接受肝臟切除手術?
A:肝臟分成左右兩葉,當腫瘤集中在某葉如右葉時,如果醫師評估開刀切除右葉腫瘤會使剩下的肝臟太小而危及生命,就不能開刀;此時改以釔90微球體放射治療將右葉腫瘤縮小後,因為肝臟有再生能力,另一葉正常肝臟覺得肝臟不夠用就會慢慢長大;肝臟變大後,就有機會接受手術治療。
vector 發表在
痞客邦
留言(0)
人氣()
資料來源與版權所有:肝病防治學術基金會
肝爹信箱有問必答(44)撰稿 / 謝佳燕(本會專業護理師)2023-10-12歡迎來電詢問
免費諮詢專線:0800-000-5831.換肝後肝癌又復發,可以再換肝或用免疫藥物治療嗎?Q:我先生年輕時就知道有B型肝炎,但沒有定期追蹤。二年前健康檢查發現肝癌後,接受過多次的電燒和栓塞,後來在朋友建議下到國外做了肝臟移植手術。術後狀況還算穩定,但不幸才一年多後肝癌又多次復發,最近超音波報告顯示肝臟有瀰漫性的腫瘤。想請問是否可以再考慮做換肝手術?標靶併免疫治療適合嗎?A:曾接受過肝臟移植手術之患者,若病情需要且經評估符合條件,可再接受第二次肝臟移植。不過,最近的檢查顯示有瀰漫性肝癌,已不適合換肝了。
至於未來的治療方式,目前肝病醫學界的共識,接受肝移植的病人有服用抗排斥藥物時,不適合接受免疫療法,故只能單獨使用標靶藥物治療。2.篩檢過B、C肝是陰性,是否不用再檢查了?Q:請問已經篩檢過B、C型肝炎且呈陰性反應,是不是一輩子就不用再篩檢了?A:一般B、C型肝炎篩檢主要是驗HBsAg(B肝表面抗原)及Anti-HCV(C肝抗體)。若HBsAg呈陰性反應,僅能代表目前血中B肝病毒量完全沒有或極微量,欲深入瞭解實際狀況,應再抽血檢驗Anti-HBs(B肝表面抗體)及Anti-HBc(B肝核心抗體),視其呈現陽性或陰性結果才能進一步具體解讀。
至於Anti-HCV呈陰性反應,僅代表過去未曾感染過C肝病毒。
雖然正常成年人日常生活中再感染B、C型肝炎病毒的機率不大,但並非絕對不會,因此即使沒有肝炎現象,仍建議至少3至5年篩檢一次。3.素食者為何還是會有三高?Q:我大伯母長期茹素,日前收到老人健檢的報告,抽血報告顯示血脂肪、血糖及肝功能都偏高很多,超音波檢查也有中度脂肪肝。令人疑惑的是,伯母身型算是偏瘦,不過,伯母平常誦經時間長,運動量不足,加上都喝蜂蜜檸檬水止渴(聽說有助酸鹼平衡)。想請問茹素的人沒有攝取動物性食物,為何還是會得到三高疾病?A:素食時,易因食材本身香氣不夠濃郁,在烹煮時常會加入較多的油來增添香氣,因此就會導致「隱性脂肪」增加,此外,素食食材來源有限,多為澱粉食材,導致澱粉攝取量過多,容易形成脂肪肝。
「類酸鹼中和」概念的飲品,因要中和過酸的口味,需加入較多的糖調味,故常飲用也會增加脂肪肝的風險。
除了飲食型態以外,運動量不足也是另一個促成脂肪肝的因素,所以要改善三高或脂肪肝,最重要的還是要從控制飲食及加強運動下手,方是解決之道。4.肝臟腺瘤會變大嗎?要切除嗎?Q:我是慢性B肝帶原者,因從事程式設計工作,常常熬夜,多年下來,體重增加很多,最近接受超音波檢查,有重度脂肪肝,此外,還有一個2.3公分的陰影,所以再安排電腦斷層查,顯示是肝臟腺瘤,請問肝臟腺瘤會變大嗎?要手術切除嗎?
A:肝臟腺瘤是良性腫瘤,形成原因目前不是很清楚,好發於女性。通常沒有症狀,也不需做任何處置。小型的肝臟腺瘤定期以超音波追蹤即可;但針對大型肝臟腺瘤,建議考慮接受手術切除,因為可能會導致內出血,也可能會破裂出血,此外,有極少的機率會轉變為惡性腫瘤。5.有B肝帶原、中度肝纖維化,是否要避免感染登革熱?Q:我爸爸是慢性B肝帶原者且已有中度肝纖維化,去年開始服用抗B肝病毒藥物貝樂克。最近聽媽媽說,隔壁阿伯感染到「登革熱」,因為爸爸每天都和阿伯下棋,請問有需要像新冠疫情一樣自我隔離嗎?A:感染到登革熱,大多數症狀都不嚴重,但根據統計,「60歲以上」、「身上有慢性病」的患者,感染登革熱,其併發症或死亡率比年輕人高,且登革熱病毒可能侵入肝臟導致嚴重程度不一的肝炎,因此慢性B肝且已有中度肝纖維化,雖有服用抗病毒藥物,還是小心謹慎為宜。
登革熱的傳染途徑是蚊子叮咬,若已出現登革熱患者,表示該地區的蚊子可能已帶有登革熱病毒,一般建議同一住家或工作場所者皆應自我監測,故建議令尊暫時不要和隔壁阿伯下棋,直到阿伯症狀消失後4周,這段期間也要做好個人及環境的防護措施。6.如何避免肝纖維化加重?Q:我小弟在竹科工作,因工作時間長,生活作息也不規律,才40歲就有中度脂肪肝,再加上他也是慢性B肝帶原者,雖說有定期追蹤,抽血報告都正常,但還是不放心。最近有自費做超音波肝纖維化檢測,結果竟顯示有嚴重的纖維化(F3)。醫師說慢性B肝帶原者及嚴重的脂肪肝也會加重肝纖維化的程度,請問此狀況要如何改善?A:肝纖維化的形成來自肝細胞發炎,令弟的肝細胞發炎可能源自B肝病毒,也可能是脂肪肝所導致,因此要定期密切追蹤血清ALT的數值。若正常,可先積極消除脂肪肝,包括在飲食和運動兩方面下功夫。若ALT數值有異常上升,則要積極與主治醫師討論是否需服用抗B肝病毒的藥物,以控制B型肝炎的病情。
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()
vector 發表在
痞客邦
留言(0)
人氣()